嵌合抗原受体在阿尔兹海默症治疗中的应用
嵌合抗原受体 (CAR) T细胞疗法是一种免疫疗法,在治疗某些类型的癌症方面表现出显著的效果。通过重新设计白细胞 (也就是 T 细胞) 上的表面蛋白,CAR-T 疗法使这些免疫细胞能够对肿瘤有吞噬作用。在某些情况下,这种创新疗法已被证明比晚期癌症的常规疗法更有效,并且已获得美国食品药品管理局 (FDA) 批准用于治疗白血病、淋巴瘤和骨髓瘤。最近,一些研究将癌细胞上的 CAR 基因靶向蛋白在巨噬细胞 (CAR-M) 中表达,用于增加其吞噬和杀灭肿瘤的能力。这类被设计的 CAR-M 在实体瘤的归巢和浸润方面已显示出优于 CAR-T 的优势。JCI Insights发表的一项新研究探讨了 CAR-M 疗法在患病率不断上升且仍然难以治疗的疾病 (如阿尔茨海默病) 中的潜在应用。
β-淀粉样蛋白的积累是阿尔茨海默病进展的关键催化剂。最初形成不溶性β-折叠,然后进一步聚集成淀粉样蛋白原纤维和斑块。这些斑块激活神经毒性级联,导致tau过度磷酸化并聚集成神经纤维缠结 (NFT) ,从而导致神经毒性和神经退化。圣路易斯华盛顿大学的研究人员表明,CAR-M技术可被用于降解致病性β-淀粉样蛋白斑块。
CAR-M 在培养物中结合并吸收β-淀粉样蛋白
为了靶向致病性β-淀粉样蛋白原纤维和斑块,研究人员首先使用 FDA 批准的用于治疗阿尔茨海默病的药物Aducanumab,以scFv (单链可变区片段) 形式设计了独特的 CAR-M 构建体 (称为β-淀粉样蛋白 CAR-M) 。在巨噬细胞中逆转录病毒表达β-淀粉样蛋白 CAR 构建体后,通过流式细胞术分析 Alexa Fluor 488 标记的StressMarq 的人源合成β-淀粉样蛋白 1-42 肽 (目录号 SPR-485 ) 的摄取情况,从而评估 CAR 功能。此阶段的观察结果令人鼓舞:β-淀粉样蛋白 CAR-M 显示出结合和重新吸收培养物中的单体β-淀粉样蛋白肽的能力, 而对应的 CAR-M 对照 (靶向 EphA2 受体) 则没有显示出这样的能力。
通过使用共聚焦显微镜监测β-淀粉样蛋白CAR-Ms 对神经毒性蛋白的吞噬作用,进一步证实了β-淀粉样蛋白的吸收。LAMP-1 共定位进一步表明β-淀粉样蛋白被降解并运输到β-淀粉样蛋白CAR-Ms 中的溶酶体区室。
此外,β-淀粉样蛋白 CAR-M 能够吸收单体、寡聚体和纤维状β-淀粉样蛋白。这是通过测量 StressMarq 的单体β-淀粉样蛋白 1-42 肽 (目录号 SPR-485 ) 、β-淀粉样蛋白 1-42 寡聚体 (目录号 SPR-488 ) 和β-淀粉样蛋白焦谷氨酸 3-42 前体原纤维 (目录号 SPR-492 ) 的吸收得出的结论。
除了识别β-淀粉样蛋白相关抗原呈递外,理想的CAR结构还应包含细胞内胞质结构域,这对于细胞信号传导功能必不可少。β-淀粉样蛋白CAR-M含有Fc受体 ( FcRγ ) 的吞噬共同γ链。对这些β-淀粉样蛋白CAR-M调节的下游分子的检查证实,CAR结构通过上调CD40和CD86等共刺激分子来实现其功能。
CAR-M可在体外减少 β 淀粉样蛋白斑块负荷
接下来,研究人员在阿尔茨海默病的 APP/PS1 小鼠模型中评估了 CAR-T 疗法的体外效果。该模型通常用于研究阿尔茨海默病病理,并且可产生大量β-淀粉样蛋白,在脑切片中很容易识别。在 APP/PS1 小鼠模型的脑切片上孵育淀粉样蛋白β CAR-M 能够显著减少斑块负担。
第一代 CAR-M 的一个局限性是,当将细胞注射到 APP/PS1 小鼠模型的海马内时,细胞的持久性有限。事实上,CAR 免疫疗法有限的持久性对患者治疗构成了挑战,并且是造成 T 细胞衰竭的主要原因。
表达 M-CSF 的β-淀粉样蛋白CAR-M 可减少海马体内斑块负荷
随后,研究人员致力于改进第一代 β-淀粉样蛋白CAR- M,并提供一种更有效的替代方案,增强体内稳定性。由于 β-淀粉样蛋白CAR-M 需要外源性细胞因子才能存活,因此开发了第二代细胞,该细胞分泌巨噬细胞集落刺激因子 (M-CSF) ——种促进巨噬细胞成熟的细胞因子。此外,在引入第二代 β-淀粉样蛋白CAR-M 之前,老年 APP/PS1 小鼠海马中的内源性小胶质细胞通过使用预处理治疗而减少。
尽管小胶质细胞在阿尔茨海默病中具有神经保护作用,但它们也能够诱导慢性促炎反应,从而导致神经毒性和神经元损伤的恶性循环。为了降低内源性小胶质细胞水平,低剂量化疗药物白消安与 CSF-1 抑制剂 PLX5622 联合使用作为预处理治疗。之后这种预处理治疗与第二代β-淀粉样蛋白CAR-Ms 相结合,得到了很好的效果。神经元细胞表现出更好的存活结果,同时体内β-淀粉样蛋白斑块负荷显著减少。
在 CAR-M 开发中使用StressMarq产品
CAR-T 细胞免疫疗法已被证明在白血病和淋巴瘤病例中非常成功,缓解率高达 93% 2。Kim等人的研究成功评估了 CAR-M 疗法是否对治疗阿尔茨海默病有效。由于这种神经退行性疾病在老龄化人口中越来越普遍,科学家们正在不断寻找新的和有前景的治疗途径。StressMarq 的单体β-淀粉样蛋白1-42 肽 (目录号 SPR-485 ) 、β-淀粉样蛋白1-42 寡聚体 (目录号 SPR-488 ) 和β-淀粉样蛋白焦谷氨酸 3-42 前体原纤维 (目录号 SPR-492 ) 使研究人员能够通过基因编辑的β-淀粉样蛋白CAR-M 检测其对β-淀粉样蛋白的吞噬作用,然后将其精进为更有效的第二代迭代。
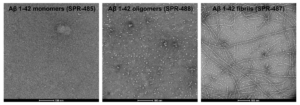
人源合成β-淀粉样蛋白1-42 单体 (目录号 SPR-485 ,左) 、低聚物 (目录号 SPR-488 ,中) 和前体原纤维 (目录号 SPR-487 ,右) 的 TEM。使用磷钨酸和醋酸铀酰染色,在碳涂层 400 目铜网上以 80 Kv采集图像。比例尺 = 100 nm。
总结
阿尔茨海默病发病机制中最早出现的病理现象之一是β-淀粉样蛋白聚集形成原纤维,并沉积在淀粉样斑块中。Kim等人发现 CAR 巨噬细胞免疫疗法具有减少β-淀粉样蛋白积累的能力,这可能对于防止阿尔茨海默病早期阶段后的疾病进展至关重要。本研究中提供的数据支持 CAR T 细胞免疫疗法在癌症治疗之外的应用,为对抗神经退行性疾病的新方法打开了大门。
相关产品信息
|
产品货号 |
产品名称 |
产品规格 |
|
SPR-485 |
Amyloid Beta Peptide 1-42 (HFIP treated) Monomers |
100 µg/500 µg/1 mg |
|
SPR-488 |
Amyloid Beta 1-42 Oligomers |
100 µg/100 µg x2/100 µg x5 |
|
SPR-492 |
Amyloid Beta Pyroglutamate 3-42 Pre-formed Fibrils |
100 µg/100 µg x2/100 µg x5 |
参考文献
- Chimeric antigen receptor macrophages target and resorb amyloid plaques. Kim, A.B. et al. JCI Insight. 2024.
- Chimeric antigen receptor T-cell therapy clinical results in pediatric and young adult B-ALL. DiNofia, A.M. & Maude, S.L. Hemasphere. 2019.
StressMarq是神经退行性疾病研究领域独特的纤维状、寡聚体和单体蛋白制剂的市场领导者。请访问StressMarq的网站或联系StressMarq中国授权代理商-欣博盛生物,了解种类繁多的tau 、β-淀粉样蛋白和α 突触核蛋白构建体的详细信息,以及相关产品的其他发表文献列表。
如需了解更多详细信息或相关产品,请联系StressMarq中国授权代理商-欣博盛生物
全国服务热线: 4006-800-892 邮箱: market@neobioscience.com
深圳: 0755-26755892 北京: 010-88594029
上海: 021-34613729 广州: 020-87615159
代理品牌网站: www.neobioscience.com
自主品牌网站: www.neobioscience.net
